Amniocentéza
Během posledních 30 let se stala amniocentéza (AMC) ve II. trimestru těhotenství rutinní metodou k vyloučení chromosomálních abnormalit u plodu. Pod kontrolou ultrazvuku může být amniocentéza snadno provedena po 15. týdnu těhotenství (obr. 4).
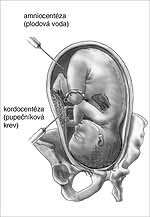
Obr. 4: Amniocentéza a kordocentéza
Za kontinuální kontroly jehly ultrazvukem se odebírá podle gestačního stáří 15–20 ml plodové vody. Buňky obsažené v plodové vodě je možno vyšetřovat cytogeneticky (stanovení karyotypu), imunofluorescenčně (genová detekce pomocí imunofluorescenčních sond) a DNA analýzou. Před cytogenetickým vyšetřením je nutná asi 10denní kultivace amniocytů, která je v dobrých laboratořích neúspěšná v méně než 1 %. Přesnost chromosomální analýzy amniocytů je 99,9%. Biochemické vyšetření plodové vody zahrnuje určení hladiny a-fetoproteinu a acetylcholinesterázy, jež je indikováno při zvýšeném riziku NTD. Úspěšnost detekce anencefalie a spina bifida je 99,5% s 0,03% falešnou pozitivitou. Riziko potratu v souvislosti s provedenou amniocentézou je asi 0,5–1 %. Zdá se, že u dvojčat je riziko poněkud vyšší. Pokud se dodržují doporučení týkající se techniky odběru, je riziko záměny mateřských a plodových buněk velmi nízké. Stejně jako ultrazvuk, tak i amniocentéza mají psychologicky pozitivní vliv u žen, kde bylo vysloveno podezření na chromosomální postižení plodu. Hlavním nedostatkem cytogenetického vyšetření je nutnost kultivace buněk trvající 14 i více dní. Imunofluorescenční vyšetření je rychlejší (diagnóza do 48 hodin), ale dává jen omezenou informaci, má nižší spolehlivost a je dražší.
V případě patologického karyotypu je možné na přání pacientky vyvolat potrat před 24. týdnem těhotenství. Tento zákrok je spojen s těžkou emocionální zátěží pacientky. Proto se hledaly a hledají další postupy, které by umožnily diagnostiku v dřívějších stadiích těhotenství.
Během posledních let byla časná amniocentéza navržena jako alternativa odběru choria (viz níže). Dodnes neexistuje přesná definice hranice mezi “konvenční” a časnou amniocentézou, ale většina pracovišť považuje odběr plodové vody před 15. týdnem těhotenství za “časný”. Bylo prokázáno zvýšené riziko malformací dolních končetin plodu (pedes equinovares) a velmi pravděpodobně i redukčních vad končetin způsobených amniálními provazci, které vzniknou traumatem amniochoriální membrány při jejím nedostatečném splynutí v časné fázi těhotenství. Proto se odběr plodové vody dnes odkládá až na dobu po 15. týdnu těhotenství.
Biopsie choria
Získání fetálních buněk v časnější fázi těhotenství umožňuje biopsie (odběr) choria (chorionic villus sampling – CVS). CVS je možno provádět od ukončeného 10. týdne (obr. 5).
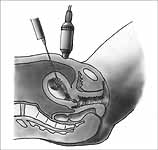
Obr. 5: Biopsie choria
Indikace CVS jsou obdobné jako u AMC. Je metodou první volby u DNA diagnostiky. CVS se stejně jako amniocentéza provádí transabdominálně, za kontinuální ultrazvukové kontroly (možný je i transcervikální odběr choria). Výhodou CVS je kratší doba kultivace než u amniocentézy. Předběžné výsledky (z krátkodobé kultivace buněk trofoblastu) jsou k dispozici během 48 hodin, konečné (z dlouhodobé kultivace mezenchymálních buněk stromatu) do 7 dnů. V dobře vedených laboratořích je cytogenetická diagnóza úspěšná až v 99,7 %. Pouze 1,1 % pacientů musí podstoupit další diagnostický test (amniocentézu nebo kordocentézu). Z toho však pouze pětina pro laboratorní selhání, ostatní pro mozaicismus nebo jiný nejednoznačný nález.
Pomocí CVS nelze na rozdíl od amniocentézy stanovit hladiny a-fetoproteinu a acetylcholinesterázy. Tento nedostatek může nahradit ultrazvukové vyšetření provedené zkušeným odborníkem na kvalitním přístroji. Riziko potratu v souvislosti s provedením biopsie choria se zdá podle současných poznatků shodné s rizikem u amniocentézy.
CVS nabývá na významu vzhledem ke snahám přesunout biochemický a ultrazvukový screening (PAPP-A, b-hCG a nuchální translucence) do I. trimestru.
Ve II. a III. trimestru těhotenství je CVS jednou z možností, jak získat vzorek tkáně plodového původu. Placentární biopsie je proveditelná i v pozdním stadiu těhotenství. Platí pro ni stejné limitace jako u CVS.
Odběr fetální krve
V současnosti se odběr fetální krve v těhotenství dělá výhradně punkcí pupečníku za přímé kontroly ultrazvuku. Riziko této metody je srovnatelné s rizikem amniocentézy. Technicky proveditelná bývá punkce až kolem 20. týdne těhotenství. Nejbezpečněji punktujeme v místě úponu pupečníku na placentu, ten se však často nezdaří vizualizovat a kordocentéza musí být provedena na volné pupečníkové kličce. Po 33. týdnu těhotenství se zvyšuje riziko bradykardie plodu v souvislosti s výkonem. Příčinou je pravděpodobně reflexní vazospazmus při nechtěné punkci umbilikální arterie.
Nejčastější indikací je potřeba rychlé karyotypizace plodu při nejasném výsledku amniocentézy nebo podezření na aneuploidii plodu vyslovené kolem 20. týdne těhotenství (srdeční vada, omfalokéla atd.), kdy by doba nutná ke kultivaci amniocytů překročila 24. týden těhotenství. Stanovení chromosomální výbavy z bílých krvinek plodu je běžnou metodou ve většině cytogenetických laboratoří a výsledky jsou k dispozici během 48–72 hodin. Diagnostická spolehlivost je velmi vysoká.
Další indikací je potřeba zjištění krevního obrazu a skupiny plodu při aloimunizaci plodu. Méně častou indikací je suspektní intrauterinní infekce, kdy se pokoušíme o přímou detekci viru či protilátek tříd IgM a IgG.
Fetální terapie v těhotenství
Většina metod antenatální intrauterinní terapie prošla fází velkého nadšení, odmítající kritiky a následně hledání opodstatněných indikací. Za fetální terapii je možno považovat ultrazvukem asistovanou intraumbilikální transfúzi (léčba erytrocytové aloimunizace; obr. 6) nebo podání trombocytárního náplavu (trombocytopenie plodu při aloimunní trombocytopenii), ale i amniodrenáž (polyhydramnion) a amnioinfúzi náhradního roztoku při oligohydramniu.
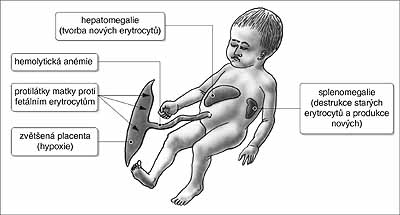
Obr. 6 : Erytrocytová aloimunizace
Syndrom vzájemné transfúze u monochoriálních dvojčat (twin-to-twin transfusion syndrome) je možno léčit laserovou koagulací cévních spojek. Jsou činěny pokusy s intrauterinní balonkovou obstrukcí trachey (fetoskopický výkon) jako prevencí plicní hypoplazie při diafragmatické hernii u plodu (nahromadění plicní tekutiny brání hypoplazii plic). Za intrauterinní terapii je možno považovat také podávání kortikoidů matce jako prevence syndromu respirační tísně plodu.
Prevence, diagnostika a léčba aloimunizace v těhotenství
Aloimunizace znamená, že matka vytváří protilátky proti krvinkám plodu, které se působením protilátek rozpadají. Nejčastěji se vyskytuje aloimunizace v systému Rh. Týká se to situací, kdy je matka Rh negativní a plod po otci zdědí Rh pozitivitu červených krvinek. Existují však imunitní konflikty i v jiných systémech než Rh. Závažnost postižení novorozenců kolísá od bezpříznakového poporodního průběhu přes povšechný otok (hydrops) až k nitroděložnímu odumření již v 18.–19. týdnu těhotenství.
Preventivní podávání anti Rh0(D) globulinu v indikovaných případech (porod Rh pozitivního plodu Rh negativní matkou, umělé ukončení těhotenství či spontánní abort starší 8 týdnů, invazivní výkony za asistence ultrazvuku v těhotenství, krvácení v těhotenství) výrazně snížilo výskyt aloimunizace v těhotenství, ale problémem zůstává inaparentní senzibilizace u Rh negativních žen pravděpodobně v důsledku více či méně fyziologické fetomaternální transfúze.
Smyslem prenatální diagnostiky u těhotných s aloimunizací je stanovit stupeň ohrožení či postižení plodu, jeho další prognózu, způsob sledování a léčení plodu. Je nutné včas rozhodnout o intrauterinní léčbě transfúzí a stanovit optimální termín porodu s ohledem jak na riziko nezralosti plic a chudokrevnosti plodu, tak na možnosti nitroděložní léčby.
